Zajímá vás problematika bakteriofágů?
Bakteriofág – odvozeno ze slov bakterie a fagein (řecky φᾶγεῖν, "jíst"), zkráceně fág, obecný název pro virus infikující bakterie.
Bakteriofágy jsou nejpočetnějším biologickým objektem v biosféře, jejich počet se odhaduje na 10³¹ částic. Můžeme je najít na všech místech osídlených jejich bakteriálními hostiteli, jako například půda nebo střeva živočichů. Jedním z nejkoncentrovanějších nalezišť fágů a dalších virů je mořská voda, ve které bylo nalezeno až 9x10⁸ virionů na mililitr a až 70 % mořských bakterií jimi může být infikováno.
Fágy byly dlouho považovány za neživé objekty, protože nemají vlastní metabolismus, nereagují na změny okolí a pro svoje rozmnožování využívají bakterie, ale v současnosti jsou oficiálně označovány jako tzv. živé nebuněčné entity.
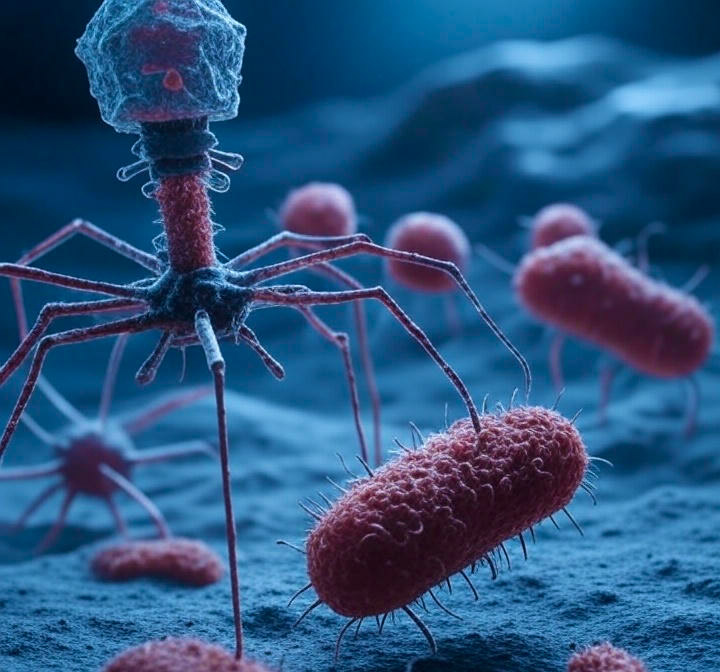
Bakteriofágy jsou výrazně menší než bakterie, jejich velikost se pohybuje obvykle mezi 20 a 200 nm. Typická stavba fágů zahrnuje bílkovinnou kapsidu a v ní uzavřený genetický materiál. Na kapsidu krčkem navazuje bičík s bičíkovou pochvou, bazální destičkou a vlákny bičíku sloužícími k přichycení na povrch bakterie. Genetický materiál je tvořen DNA nebo RNA, a to jednovláknová i dvouvláknová, kružnicová i lineární, dlouhá 5 000 až 500 000 nukleotidů.
Pojďme se podívat na historii a srovnání s antibiotiky:
V roce 1896 publikoval chemik E. H. Hankin prostřednictvím Pasteurova institutu aktivitu neznámého zdroje v řece Ganga, která ničí bakterii Vibrio chalerae způsobující choleru. V roce 1915 pak britský mikrobiolog Frederick W. Twort izoloval objekty, které byly o několik let později nazvány bakteriofágy - totiž „požírači bakterií“. Kromě Tworta se na objevu bakteriofágů podílel i francouzsko-kanadský mikrobiolog Félix d´Hérelle, který fágy izoloval v roce 1917 nezávisle na něm a později je úspěšně použil k léčbě úplavice (právě on je autorem termínu bakteriofág).
Po 60 let byly fágy užívány v Sovětském svazu jako alternativa k antibiotikům. Po objevení penicilinu a jeho zavedení do klinické praxe se však pozornost zaměřila na antibiotika a fágy ustoupily do pozadí. Jejich výzkum se udržel jedině v bývalém Sovětském svazu, zejména v Eliavově institutu v gruzínském Tbilisi, který funguje dodnes a vyrábí bakteriofágové preparáty k léčbě bakteriálních infekcí. V současnosti však fágy zažívají celosvětový "comeback", zejména kvůli neustále rostoucímu počtu multirezistentních kmenů bakterií (např. Staphylococcus aureus, Pseudomonas aeruginosa, atd.).
Známé bakteriofágy jsou morfologicky velmi rozmanité, jejich symetrie je ikozahedrální (20 rovnostranných trojúhelníků = mají tvar kapsidy) nebo helikální (tvar šroubovice, spirály), případně obě.
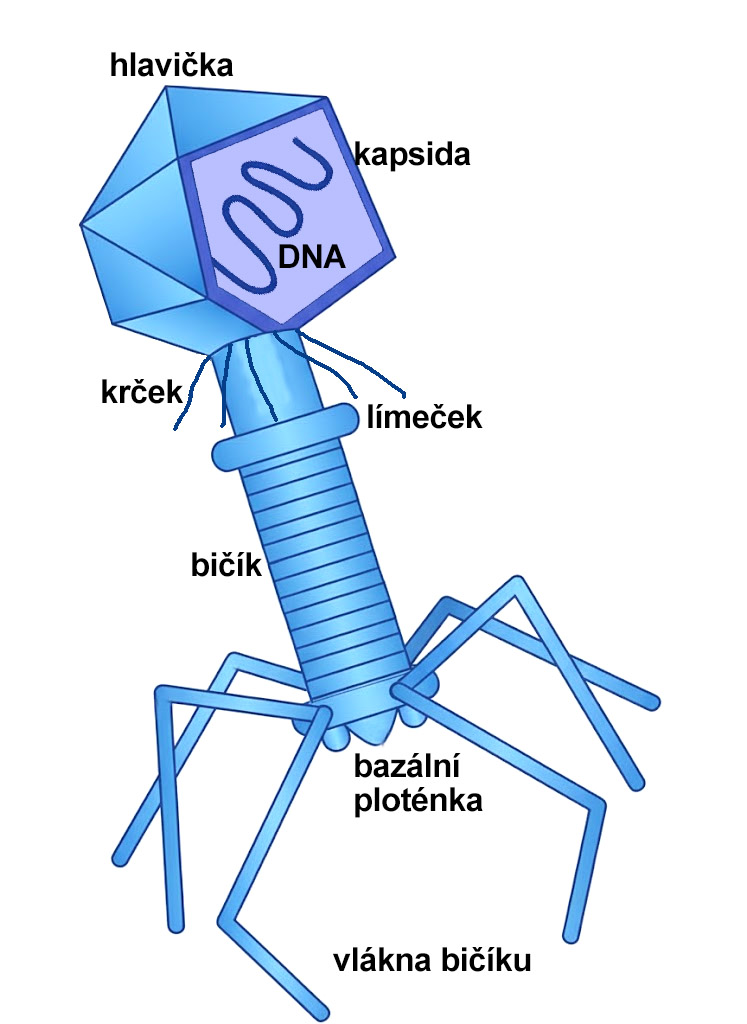
U největších a nejsložitějších bakteriofágů (např. bakteriofágy Escherichia coli T2, T4 a T6) vykazuje hlavička symetrii ikozahedrální a bičík helikální. Průměr hlavičky různých bakteriofágů se pohybuje v rozmezí 15 – 100 nm, délka bičíků je různá (od sotva patrného, po asi 200 nm), průměr bičíku je 10 nm.
Z velkých fágů má např. fág T4 hlavičku o průměru asi 65 nm a délce 95 nm. Hlavička má tvar dvou polovičně příčně rozdělených ikozahedrů spojených nízkým šestibokým hranolem. Bičík, dlouhý také 95 nm, je pevný, ale jeho povrchová pochva je kontraktilní. Na konci bičíku je připojena šestiboká bazální ploténka s ostny a bičíkovými vlákny. Osou bičíku prochází dutá dřeň. Liché bakteriofágy téže řady (T1, T3) mají dlouhé a ohebné bičíky, bez kontraktilní složky. Bičík bakteriofága nikdy neslouží k pohybu.
Malé ikozahedrální bakteriofágy se dále rozdělují do dvou typů podle toho, zda mají nebo nemají velké, hroty opatřené kapsomery (základní proteinová strukturní jednotka tvořící kapsidu viru) ve všech dvanácti rozích svého ikozahedru.
Tyčinkové bakteriofágy obsahují buď jednořetězcovou DNA nebo RNA. Nejmenší bakteriofágy s jednořetězcovou RNA jsou kulovitého tvaru; jen o něco větší bakteriofágy s jednořetězcovou DNA jsou buď dvanáctistěnné nebo vláknité.
Klasifikace bakteriofágů
Dosavadní pokusy o zavedení morfologické klasifikace rozlišují 5 základních typů bakteriofágů:
- virion ikozahedrický a stažitelného (kontraktilního) bičíku
- virion ikozahedrický s nestažitelným bičíkem
- virion ikozahedrický bez bičíku
- virion tyčinkovitý až vláknitý
- virion kulovitý hlavičky
Podle průběhu životního cyklu lze bakteriofágy rozdělit do dvou skupin:
- fágy virulentní s lytickým životním cyklem
- fágy temperované s lyzogenním životním cyklem
Virulentní fágy s lytickým životním cyklem
Tyto bakteriofágy způsobují lýzu hostitelské bakteriální buňky. Jejich životní cyklus začíná adsorpcí virionu na povrch vnímavé buňky (u grampozitivních bakterií fágy nasedají obvykle na teichoové kyseliny), následuje penetrace nukleové kyseliny fága do cytoplazmy buňky a její replikace s využitím DNA polymerázy hostitele. V dalším kroku vzniká raná fágová mRNA a jsou syntetizovány proteiny kontrolující jejich syntézu a následně se syntetizují také tzv. pozdní bílkoviny fága. Po nasyntetizování potřebných složek jsou kompletovány nové virové částice (viriony), které se uvolní do vnějšího prostředí (pomozí endolyzinů dochází k lýze bakteriální buňky). Uvolněné viriony mohou následně infikovat další citlivé buňky.
Virulentní fágy - způsob replikace:
- navázání na hostitelskou buňku,
- vpravení genetické informace,
- replikace DNA/RNA a syntéza proteinů,
- kompletace nových virionů,
- lýze buňky pomocí enzymů (endolyzinů)
Temperované fágy s lyzogenním cyklem
Tyto fágy se rekombinací začleňují do genomu hostitele, jejich nukleová kyselina se replikuje a přenáší na potomstvo spolu s genomem bakteriální buňky. Takto začleněný fág se nazývá profág. Působením některých vnějších faktorů (např. UV záření, mutageny, stresové faktory) se profág může opět uvolnit a vyčlenit z nukleové kyseliny bakteriální buňky a temperovaný fág se stane fágem virulentním. Při chybném vyčlenění se může spolu s genetickou informací fága vyčlenit i část genomu hostitelské bakterie, která se tak stane součástí nové virové částice a může být šířena dál. Tento proces se nazývá transdukce a např. u druhu Staphylococcus aureus je nejčastějším způsobem horizontálního přenosu genů.
Temperované fágy - způsob replikace:
- genetická informace se začleňuje do genomu bakterie jako profág,
- profág se přenáší při dělení hostitele,
- vlivem stresových faktorů (UV záření, mutageny) může přejít zpět do lytického cyklu,
- při chybné excizi může dojít k přenosu bakteriálních genů – proces transdukce.
Princip účinků bakteriofágů
Lytické fágy jsou nejefektivnější, protože způsobují lýzu cílových bakterií (žlutě orámováno).
Bakteriofágy jsou schopné lyzovat napadené bakterie, mohou proto sloužit jako účinná antibakteriální léčiva. Problém je v tom, že každý druh bakteriofága napadá jen konkrétní druh bakterie, ve velké většině případů však pouze několik kmenů v rámci tohoto druhu. Aby byla léčba účinná, musí se nejprve přesně určit konkrétní bakteriální druh a kmen, který způsobil infekci, a pak podat pacientovi přesně vybrané bakteriofágy.
Léčba pomocí bakteriofágů je tedy časově náročnější než např. použití širokospektrálních antibiotik. Ovšem vzhledem k tomu, že v současnosti je již mnoho bakteriálních kmenů rezistentních vůči nejméně jednomu antibiotiku. Některé nemocniční kmeny Staphylococcus aureus (lidově "zlatý stafylokok") jsou rezistentní vůči všem běžně používaným antibiotikům včetně vankomycinu, který je tzv. antibiotikem první volby u komplikovaných infekcí, se nakonec fágy ukazují jako lepší varianta a jejich využití má velký potenciál.
Fágová terapie má oproti antibiotikům mnoho velkých výhod, např.:
- Bakterie si v dlouhodobém horizontu nedokážou vytvořit rezistenci k bakteriofágům, protože fágy taktéž mutují a některé z těchto mutací pomohou překonat bakteriální rezistenci („nikdy nekončící závod“)
- Fágy jsou vysoce specifické, konkrétní fág (nebo úzká skupina fágů) je schopen infikovat pouze konkrétní bakteriální kmen (nebo úzkou skupinu kmenů), a tak chrání mikroflóru organismu.
- Příprava a výroba bakteriofágových preparátů je mnohem levnější než zavedení nového antibiotika.
- Produkce fágových preparátů je taktéž nesrovnatelně rychlejší než zavádění nových antibiotik.
Bakteriofágy
Výhody:
- Vysoká specifita – cíleně ničí jen konkrétní bakterii, nepoškozují přirozenou mikroflóru (např. ve střevech).
- Množení v místě infekce – pokud jsou přítomny cílové bakterie, fágy se dále samy množí.
- Účinnost proti rezistentním bakteriím – mohou ničit bakterie odolné vůči antibiotikům.
- Možnost personalizace – lze vyvinout fágovou terapii na míru konkrétnímu pacientovi.
Nevýhody:
- Nutnost přesné identifikace bakterie – fágy účinkují jen na konkrétní patogen.
- Zdlouhavý vývoj – nalezení správného fágového kmene může trvat.
- Omezená dostupnost – v západní medicíně zatím není fágová terapie běžně používaná.
- Imunitní reakce – tělo si může vytvořit protilátky proti fágům.
Antibiotika
Antibiotika jsou látky (přírodní nebo syntetické), které zabíjejí bakterie nebo brání jejich množení.
Výhody:
- Široké spektrum účinku – jedno antibiotikum často účinkuje proti více druhům bakterií.
- Rychlá dostupnost – běžně používaná v praxi, často nasazena ihned.
- Snadné použití – známé dávkování, široká klinická zkušenost.
Nevýhody:
- Rezistence – nadměrné užívání vede k rozvoji bakteriální odolnosti.
- Nežádoucí účinky – může narušit rovnováhu mikroflóry, způsobit průjmy nebo jiné komplikace.
- Nezacílenost – zabíjí i prospěšné bakterie.
Aktuální výzkum a klinické studie
V České republice probíhá několik výzkumných projektů zaměřených na bakteriofágovou terapii,hodně z nich je zaměřeno na Staphylococcus aureus.
Mezinárodní kontext
V rámci Evropské unie se bakteriofágová terapie stále nachází ve fázi výzkumu a vývoje. V některých zemích, jako je Belgie, byly vyvinuty protokoly pro magistrální přípravu fágů, které umožňují jejich individuální výrobu a použití. Fundación Rafael del Pino
V České republice se bakteriofágová terapie zatím používá především v rámci klinických studií a výzkumných projektů. Je však zřejmé, že zájem o tuto oblast roste a v budoucnu by mohla být součástí standardní léčby bakteriálních infekcí.
Zdroje:
1. Wikipedie
2. VIRY A BAKTERIOFÁGY V POTRAVINÁCH - Iveta Vaňková, Veronika Čurečková MVDr. Šárka Bursová, Ph.D., 2018, VFU Brno